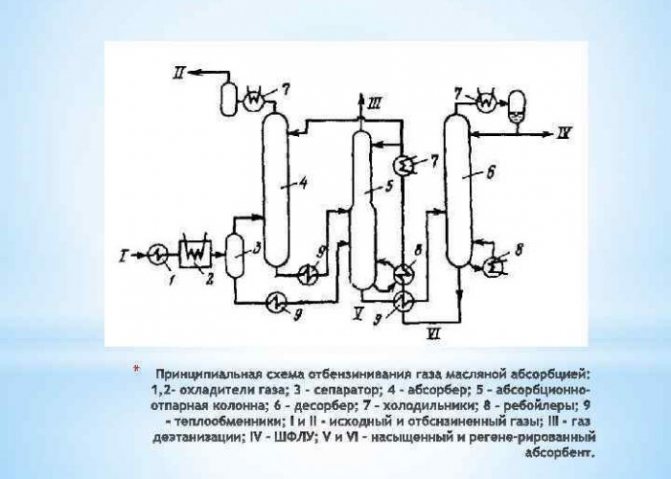
Metode de producere a hidrogenului în condiții industriale
Extracția prin conversie de metan
... Apa în stare de vapori, preîncălzită la 1000 grade Celsius, este amestecată cu metan sub presiune și în prezența unui catalizator. Această metodă este interesantă și dovedită, de asemenea, trebuie remarcat faptul că este în mod constant îmbunătățit: este în curs de căutare noi catalizatori, mai ieftini și mai eficienți.
Luați în considerare cea mai veche metodă de producere a hidrogenului - gazeificarea cărbunelui
... Dacă nu există acces la aer și o temperatură de 1300 grade Celsius, cărbunele și vaporii de apă sunt încălziți. Astfel, hidrogenul este deplasat din apă și se obține dioxid de carbon (hidrogenul va fi în partea de sus, dioxidul de carbon, obținut și ca urmare a reacției, este în partea de jos). Aceasta va fi separarea amestecului de gaze, totul este foarte simplu.
Obținerea hidrogenului prin electroliza apei
este considerată cea mai simplă opțiune. Pentru punerea sa în aplicare, este necesar să turnați o soluție de sodă în recipient și să plasați acolo două elemente electrice. Unul va fi încărcat pozitiv (anod), iar celălalt negativ (catod). Când se aplică curent, hidrogenul va merge la catod și oxigenul la anod.
Obținerea hidrogenului prin metodă oxidare parțială
... Pentru aceasta, se folosește un aliaj de aluminiu și galiu. Este plasat în apă, ceea ce duce la formarea de hidrogen și alumină în timpul reacției. Galiul este necesar pentru ca reacția să aibă loc în întregime (acest element va împiedica oxidarea prematură a aluminiului).
Relevanță dobândită recent metoda de utilizare a biotehnologiei
: în condiția lipsei de oxigen și sulf, chlamydomonasul începe să elibereze intens hidrogen. Un efect foarte interesant, care acum este studiat activ.

Nu uitați o altă metodă veche, dovedită de producere a hidrogenului, care constă în utilizarea diferitelor elemente alcaline
si apa. În principiu, această tehnică este fezabilă în laborator, cu măsurile de siguranță necesare. Astfel, în cursul reacției (se continuă cu încălzirea și cu catalizatorii), se formează un oxid metalic și hidrogen. Rămâne doar să-l colectăm.
Obțineți hidrogen interacțiunea apei și a monoxidului de carbon
posibil doar într-un mediu industrial. Se formează dioxid de carbon și hidrogen, principiul separării lor este descris mai sus.

INVENȚIA CONȚINE URMĂTOARELE AVANTAJE
Căldura obținută prin oxidarea gazelor poate fi utilizată direct la fața locului, iar hidrogenul și oxigenul se obțin din eliminarea aburului rezidual și a apei de proces.
Consum redus de apă la generarea de energie electrică și căldură.
Simplitatea drumului.
Economii semnificative de energie ca se cheltuiește numai pentru încălzirea starterului la regimul termic stabilit.
Productivitate ridicată a procesului, deoarece disocierea moleculelor de apă durează zecimi de secundă.
Siguranța la explozie și la incendiu a metodei, deoarece în implementarea sa, nu este nevoie de containere pentru colectarea hidrogenului și oxigenului.
În timpul funcționării instalației, apa este purificată în mod repetat, fiind transformată în apă distilată. Aceasta elimină sedimentele și calcarul, ceea ce crește durata de viață a instalației.
Instalația este realizată din oțel obișnuit; cu excepția cazanelor din oțeluri rezistente la căldură cu căptușeală și ecranare a pereților lor. Adică nu sunt necesare materiale scumpe speciale.
Invenția își poate găsi aplicația în
industria prin înlocuirea hidrocarburilor și combustibilului nuclear din centralele electrice cu apă ieftină, răspândită și ecologică, menținând în același timp puterea acestor centrale.
Arderea hidrogenului
Prin urmare, hidrogenul dă naștere apei. Apa se obține prin arderea hidrogenului - prin combinarea hidrogenului cu oxigenul. O cantitate foarte mare de energie este eliberată în timpul reacției.
2H2 + O2 = 2H2O + Q
Aceasta înseamnă că hidrogenul poate fi folosit ca combustibil. Și, ca în cazul oricărui combustibil, hidrogenul trebuie manipulat cu grijă.
Obținem hidrogen prin reacția zincului cu acidul clorhidric.
Aprindem hidrogenul la capătul tubului de evacuare a gazului. La început, flacăra este abia vizibilă (hidrogenul nu colorează flacăra). Treptat, tubul de sticlă devine fierbinte și flacăra devine galbenă: compușii de sodiu care alcătuiesc sticla colorează flacăra.
Smochin. 2. Arderea hidrogenului
Deci hidrogenul este combustibil. Motoarele cu reacție pot funcționa cu hidrogen și oxigen. Căldura de reacție a arderii hidrogenului este utilizată pentru sudarea și tăierea metalelor. Când hidrogenul arde în oxigen pur, temperatura ajunge la 2800 ° C. Această flacără topește cuarțul și majoritatea metalelor. Este important ca hidrogenul să fie un combustibil ecologic. produsul combustiei sale este apa.
REVENDICARE
Metoda de producere a hidrogenului și a oxigenului din vaporii de apă
, inclusiv trecerea acestui abur printr-un câmp electric, caracterizat prin aceea că utilizează abur de apă supraîncălzit cu o temperatură
500 - 550 o C
, a trecut printr-un câmp electric de înaltă tensiune cu curent continuu pentru a disocia vaporii și a-l separa în atomi de hidrogen și oxigen.
De mult am vrut să fac un lucru similar. Dar alte experimente cu o baterie și o pereche de electrozi nu au ajuns. Am vrut să fac un aparat cu drepturi depline pentru producerea de hidrogen, în cantități, pentru a umfla un balon. Înainte de a face un aparat complet pentru electroliza apei acasă, am decis să verific totul pe model.
Schema generală a electrolizatorului arată astfel.
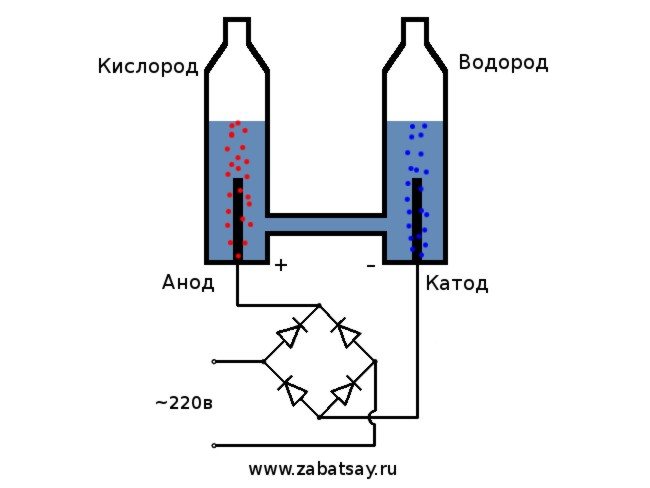

Acest model nu este potrivit pentru utilizarea zilnică completă. Dar am reușit să testăm ideea.
Așa că am decis să folosesc grafit pentru electrozi. O sursă excelentă de grafit pentru electrozi este colectorul de troleibuz. Există o mulțime de oameni care stau în jurul valorii de la opriri. Trebuie amintit că unul dintre electrozi se va prăbuși.


Am văzut și finalizat cu un fișier. Intensitatea electrolizei depinde de puterea curentului și de aria electrozilor.


Sârmele sunt atașate la electrozi. Firele trebuie izolate cu grijă.


Pentru cazul modelului de electrolizator, sticlele din plastic sunt destul de potrivite. Găurile sunt realizate în capac pentru conducte și fire.


Totul este bine acoperit cu etanșant.


Gâturile de sticlă tăiate sunt potrivite pentru conectarea a două containere.


Acestea trebuie unite și cusătura trebuie topită.


Nucile sunt fabricate din capace pentru sticle.


Găurile sunt realizate în două sticle în partea de jos. Totul este conectat și umplut cu atenție cu etanșant.


Vom folosi o rețea de uz casnic de 220V ca sursă de tensiune. Vreau să te avertizez că aceasta este o jucărie destul de periculoasă. Deci, dacă nu aveți suficiente abilități sau există îndoieli, atunci este mai bine să nu repetați. În rețeaua menajeră, avem un curent alternativ, pentru electroliză trebuie îndreptat. Un pod cu diode este perfect pentru aceasta. Cel din fotografie nu era suficient de puternic și a ars rapid. Cea mai bună opțiune a fost podul chinezesc cu diode MB156 într-o carcasă din aluminiu.


Puntea diodei se încălzește foarte tare. Va fi necesară răcirea activă. Un cooler pentru un procesor de computer este perfect. O cutie de joncțiune de o dimensiune adecvată poate fi utilizată pentru incintă. Vândut în articole electrice.


Mai multe straturi de carton trebuie așezate sub puntea diodei.


Găurile necesare sunt făcute în capacul cutiei de joncțiune.


Așa arată unitatea asamblată. Electrolizorul este alimentat de la rețea, ventilatorul este alimentat de o sursă de alimentare universală. O soluție de bicarbonat de sodiu este utilizată ca electrolit. Aici trebuie amintit că, cu cât concentrația soluției este mai mare, cu atât este mai mare viteza de reacție. Dar, în același timp, încălzirea este, de asemenea, mai mare. Mai mult, reacția de descompunere a sodiului la catod va contribui la încălzire. Această reacție este exotermă. Ca rezultat, se vor forma hidrogen și hidroxid de sodiu.


Dispozitivul din fotografia de mai sus era foarte fierbinte. Trebuia oprit periodic și așteptați până se răcește. Problema încălzirii a fost parțial rezolvată prin răcirea electrolitului. Pentru aceasta am folosit o pompă de fântână de masă. Un tub lung trece de la o sticlă la alta printr-o pompă și o găleată cu apă rece.


Relevanța acestui număr astăzi este destul de mare datorită faptului că sfera utilizării hidrogenului este extrem de extinsă și, în forma sa pură, practic nu se găsește nicăieri în natură. De aceea au fost dezvoltate mai multe tehnici care permit extragerea acestui gaz din alți compuși prin reacții chimice și fizice. Acest lucru este discutat în articolul de mai sus.
Lecția Lucrare practică „Obținerea hidrogenului și studierea proprietăților acestuia”.
Lecția 31 Clasa 8 -
Subiect:
Lucrare practică nr. 4 Obținerea hidrogenului și studierea proprietăților acestuia.
Data ____________20
MBOU "S (K) OSH №16", profesor de chimie Berezinskaya A.A.
Scop:
- îmbunătățirea abilităților experimentale - tehnici de lucru cu echipamente și substanțe de laborator; capacitatea de a observa, trage concluzii, întocmi rezultatele muncii practice în caiete;
- lucrați la dezvoltarea abilităților în manipularea cu îndemânare a focului, a substanțelor periculoase.
- capacitatea de a întocmi ecuații ale reacțiilor chimice, capacitatea de a trage concluzii, de a respecta regulile de siguranță;
- lărgirea orizontului studenților, construirea respectului pentru istoria științei.
- dezvoltarea de idei despre un stil de viață sănătos în blocuri: „Chimia în viața de zi cu zi - un comportament sigur”.
Obiective corective:
corectarea și dezvoltarea vorbirii coerente orale și scrise, corectarea și dezvoltarea memoriei motorii, dezvoltarea capacității de a trage concluzii.
Echipament:
- suport de laborator cu picior, suport pentru eprubetă, suport pentru eprubete, lingură dozatoare, hârtie de filtru
- lampă spirtoasă, chibrituri
- dispozitiv automat Kiryushkin pentru obținerea gazelor, 3 eprubete, cristalizator cu apă
Reactivi:
granule de zinc, acid clorhidric (diluat), oxid de cupru (II).
Tipul lecției
: lecție practică (laborator virtual)
Norme de siguranță:
Lucrul cu o lampă spirtoasă; lucrați cu sticlă; Verificarea dispozitivului pentru scurgeri.
Progres:
I. Pregătirea pentru munca practică.
- Informare privind siguranța la lucrul cu combustibil uscat.
- Informare tehnică cu privire la modul de desfășurare a lucrărilor practice.
II. Actualizarea cunoștințelor
- Ce materii prime vom folosi pentru a obține hidrogen?
- Amestecul de reacție trebuie încălzit?
- Ce trebuie să căutați atunci când înregistrați observații?
- Ce dispozitiv vom folosi pentru a produce hidrogen?
- Ce metode pot fi folosite pentru colectarea hidrogenului, de ce?
Cunoașterea instrucțiunii: pagina tutorial ________
III. Lucrări practice (vizionarea videoclipului: Producția de hidrogen.)
III. Consolidarea cunoștințelor, abilităților, abilităților.
După efectuarea lucrării, trageți o concluzie, notați toate rezultatele într-un caiet.
Teme pentru acasă: § ________.
Lucrări practice nr. 4. Producerea hidrogenului și studiul proprietăților acestuia.
Cunosc regulile de siguranță
Scop:
învățați să primiți, să colectați hidrogen; studiază proprietățile fizice și chimice ale hidrogenului.
Echipament:
raft de laborator cu picior, suport pentru eprubete, suport pentru eprubete, lingură dozatoare, hârtie de filtru, lampă cu alcool, chibrituri, dispozitiv automat Kiryushkin pentru obținerea gazelor, 3 eprubete, un cristalizator cu apă.
Reactivi:
granule de zinc, acid clorhidric (diluat), oxid de cupru (II).
Progres
1. O metodă de producere a hidrogenului - interacțiunea metalelor active cu acizii.
Zn + 2HCl = ZnCl2 + H2 ↑ + Q - în condiții normale
Observații:
- reacția interacțiunii granulelor de zinc cu acidul clorhidric se desfășoară lent la început, apoi foarte violent, eprubeta se încălzește
- gazul incolor scapă din conducta de evacuare a gazului
- când soluția rezultată este evaporată, rămâne o pulbere albă pe placa de sticlă
2. Dispozitive pentru obținerea și colectarea hidrogenului
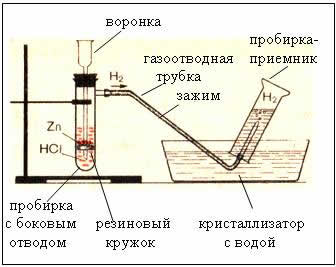

Smochin. Dispozitivul pentru producerea hidrogenului este automat, ceea ce vă permite să opriți reacția în orice moment folosind o clemă (dispozitivul lui Kiryushkin).
Colectarea gazului prin deplasarea apei este posibilă deoarece hidrogenul este ușor solubil în el.
- prin urmare, hidrogenul este mai ușor decât aerul
3. Detectarea hidrogenului - verificarea purității acestuia
Observații:
- când prima porție de gaz este arsă, se aude un sunet aspru de lătrat
- la arderea celei de-a doua porții de gaz se aude un bumbac ușor Figura 5
"P-inghinal"
4. Proprietatea hidrogenului este un agent activ de reducere
Observații:
- pulberea își schimbă culoarea din negru în cupru
- pe pereții eprubetei apar picături de lichid incolore
Ieșire:
Una dintre modalitățile de a obține hidrogen în laborator este interacțiunea zincului cu acidul clorhidric diluat, care formează o sare (clorură de zinc) și hidrogen. Hidrogenul este un gaz incolor, inodor, ușor solubil în apă, mai ușor decât aerul, exploziv amestecat cu aer, reduce metalele din oxizii lor.
3
Producția de hidrogen de uz casnic
Selectarea electrolizatorului
Pentru a obține un element al casei, aveți nevoie de un aparat special - un electrolizator. Există multe opțiuni pentru astfel de echipamente pe piață; dispozitivele sunt oferite atât de corporații tehnologice bine cunoscute, cât și de producători mici. Unitățile de marcă sunt mai scumpe, dar calitatea construcției este mai mare.
Aparatul de uz casnic este mic și ușor de utilizat. Principalele sale detalii sunt:
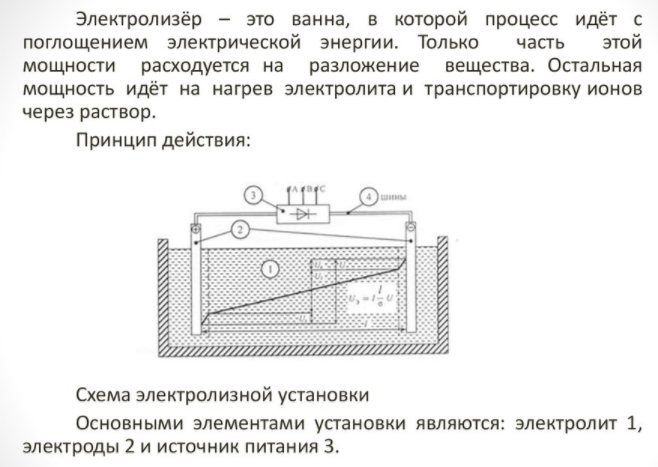

Electrolizator - ce este
- reformator;
- sistem de curatare;
- celule de combustibil;
- echipamente pentru compresoare;
- un recipient pentru stocarea hidrogenului.
Apa simplă de la robinet este luată ca materie primă, iar electricitatea provine dintr-o priză obișnuită. Unitățile alimentate cu energie solară economisesc energie electrică.
Hidrogenul de acasă este utilizat în sistemele de încălzire sau gătit. Și, de asemenea, îmbogățesc amestecul combustibil-aer pentru a crește puterea motoarelor mașinii.
Realizarea unui aparat cu propriile mâini
Este chiar mai ieftin să faci dispozitivul singur acasă. O celulă uscată arată ca un recipient sigilat, care constă din două plăci de electrod într-un recipient cu o soluție electrolitică. World Wide Web oferă o varietate de scheme de asamblare pentru dispozitive de diferite modele:
- cu două filtre;
- cu dispunerea superioară sau inferioară a containerului;
- cu două sau trei supape;
- cu placa zincata;
- pe electrozi.
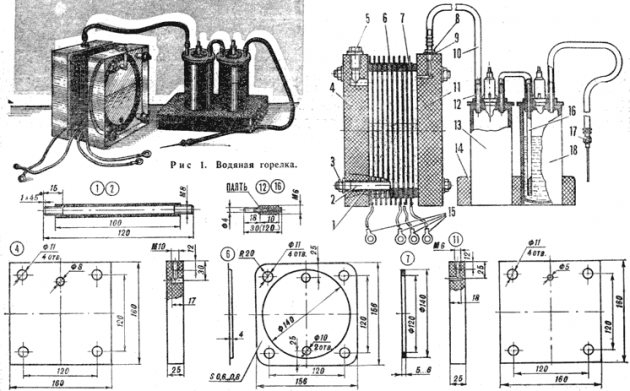

Diagrama dispozitivului de electroliză
Nu este dificil să creezi un dispozitiv simplu pentru producerea hidrogenului. Va necesita:
- tabla de otel inoxidabil;
- tub transparent;
- fitinguri;
- recipient din plastic (1,5 l);
- filtru de apă și supapă de reținere.
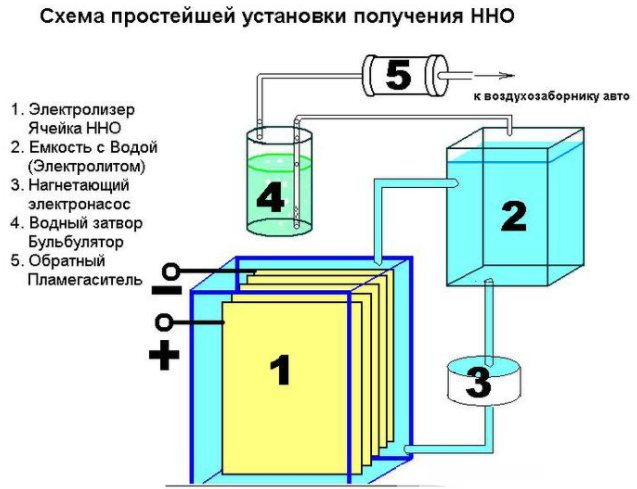

Dispozitivul unui dispozitiv simplu pentru producerea hidrogenului
În plus, vor fi necesare diverse componente hardware: piulițe, șaibe, șuruburi. Primul pas este să tăiați foaia în 16 compartimente pătrate, tăiați un colț din fiecare dintre ele. În colțul opus de acesta, trebuie să găuriți o gaură pentru șurubarea plăcilor. Pentru a asigura un curent constant, plăcile trebuie conectate conform schemei plus - minus - plus - minus. Aceste părți sunt izolate unele de altele cu un tub și la conexiunea cu un șurub și șaibe (trei piese între plăci). 8 plăci sunt plasate pe plus și minus.
Când sunt asamblate corespunzător, coastele plăcilor nu vor atinge electrozii. Piesele asamblate sunt coborâte într-un recipient din plastic. În punctul în care pereții se ating, două găuri de montare sunt realizate cu șuruburi. Instalați o supapă de siguranță pentru a elimina excesul de gaz. Fitingurile sunt montate în capacul recipientului, iar cusăturile sunt sigilate cu silicon.
Testarea aparatului
Pentru a testa dispozitivul, efectuați mai multe acțiuni:
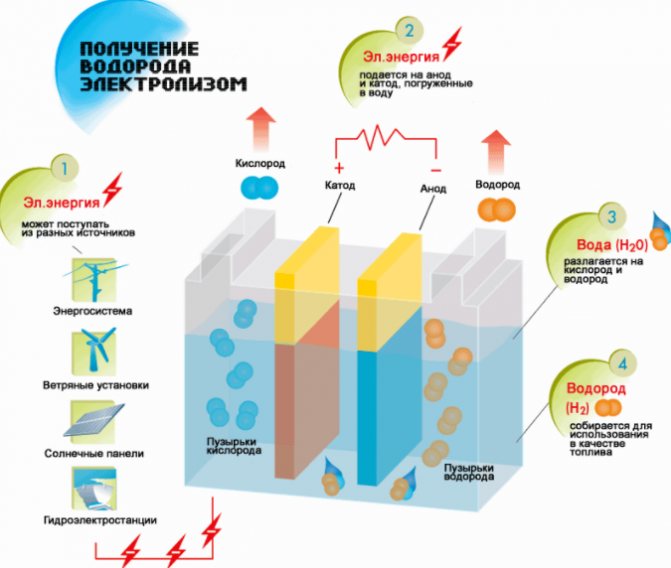

Schema de producere a hidrogenului
- Umpleți cu lichid.
- Acoperind cu un capac, conectați un capăt al tubului la fiting.
- Al doilea este scufundat în apă.
- Conectați-vă la o sursă de alimentare.
După conectarea dispozitivului la o priză, după câteva secunde, procesul de electroliză și precipitațiile vor fi vizibile.
Apa pură nu are o conductivitate electrică bună. Pentru a îmbunătăți acest indicator, trebuie să creați o soluție electrolitică prin adăugarea unui hidroxid de sodiu alcalin. Se găsește în compuși de curățare a țevilor, cum ar fi Mole.
Cum funcționează dispozitivul
Electrolizorul este format din mai multe plăci metalice scufundate într-un recipient sigilat cu apă distilată.
Corpul în sine are terminale pentru conectarea sursei de alimentare și există o bucșă prin care se descarcă gazul.
Funcționarea dispozitivului poate fi descrisă după cum urmează: un curent electric este trecut prin apă distilată între plăci cu câmpuri diferite (una are un anod, cealaltă are un catod), o împarte în oxigen și hidrogen.
În funcție de suprafața plăcilor, curentul electric are propria putere, dacă suprafața este mare, atunci mult curent trece prin apă și se eliberează mai mult gaz. Diagrama de conectare a plăcilor este alternativă, mai întâi plus, apoi minus și așa mai departe.
Se recomandă ca electrozii să fie din oțel inoxidabil, care nu reacționează cu apa în timpul procesului de electroliză. Principalul lucru este să găsești oțel inoxidabil de înaltă calitate. Mai bine faceți distanța dintre electrozi mică, dar astfel încât bulele de gaz să se poată deplasa cu ușurință între ele. Este mai bine să realizați elemente de fixare din metalul corespunzător ca electrozi.
În acest exemplu de realizare, dispozitivul include 16 plăci, acestea sunt situate la 1 mm unul de celălalt.
Datorită faptului că plăcile au o suprafață și o grosime destul de mari, va fi posibil să treacă curenți mari printr-un astfel de dispozitiv, dar metalul nu se va încălzi. Dacă măsurăm capacitatea electrozilor în aer, atunci va fi 1nF, acest set folosește până la 25A în apă simplă de la rețea.
Pentru a colecta un generator de hidrogen cu propriile mâini, puteți utiliza un recipient pentru alimente, deoarece plasticul său este rezistent la căldură. Apoi, trebuie să coborâți electrozii pentru colectarea gazului cu conectori izolați ermetic, un capac și alte conexiuni în recipient.
Dacă utilizați un recipient din metal, atunci pentru a evita un scurtcircuit, electrozii sunt atașați la plastic. Pe ambele părți ale armăturilor din cupru și alamă sunt montați doi conectori (montaj - montare, asamblare) pentru extragerea gazului. Conectorii și armăturile de contact trebuie să fie fixate ferm folosind un material de etanșare din silicon.
De asemenea, puteți face un generator de gaz acasă. Tehnica este detaliată aici:
Metode de producere a hidrogenului
Hidrogenul este un element gazos incolor și inodor cu o densitate de 1/14 față de aer. Într-un stat liber, este rar. De obicei hidrogenul este combinat cu alte elemente chimice: oxigen, carbon.
Producția de hidrogen pentru necesități industriale și electrotehnică se realizează prin mai multe metode. Cele mai populare sunt:
- electroliza apei;
- metoda de concentrare;
- condens de temperatură scăzută;
- adsorbţie.
Hidrogenul poate fi izolat nu numai de compuși gazoși sau de apă. Hidrogenul este produs prin expunerea lemnului și cărbunelui la temperaturi ridicate, precum și prin prelucrarea deșeurilor biologice.
Hidrogenul atomic pentru inginerie electrică se obține folosind metoda disocierii termice a unei substanțe moleculare pe un fir realizat din platină, tungsten sau paladiu. Este încălzit într-o atmosferă de hidrogen la o presiune mai mică de 1,33 Pa. Și, de asemenea, elementele radioactive sunt folosite pentru a produce hidrogen.
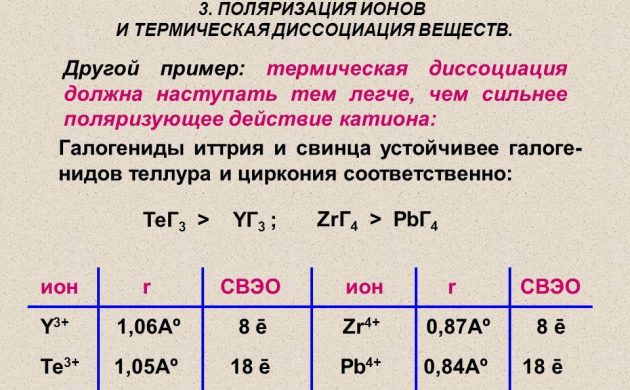

Disocierea termică
Metoda electrolizei
Cea mai simplă și mai populară metodă de evoluție a hidrogenului este electroliza apei. Permite producerea de hidrogen practic pur.Alte avantaje ale acestei metode sunt:
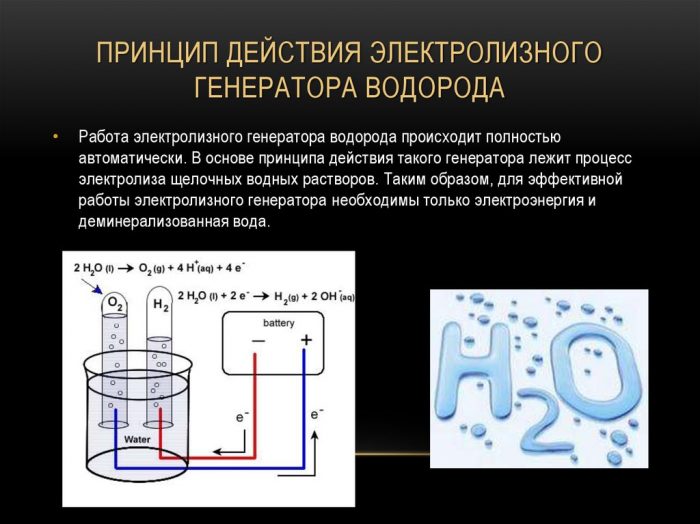

Principiul de funcționare al generatorului de hidrogen de electroliză
- disponibilitatea materiilor prime;
- primirea unui element sub presiune;
- capacitatea de a automatiza procesul din cauza lipsei pieselor mobile.
Procedura de divizare a unui lichid prin electroliză este inversul arderii hidrogenului. Esența sa este că sub influența curentului continuu, oxigenul și hidrogenul sunt eliberați pe electrozii înmuiați într-o soluție apoasă de electroliți.
Un avantaj suplimentar este considerat a fi producția de subproduse cu valoare industrială. Astfel, este necesară o cantitate mare de oxigen pentru a cataliza procesele tehnologice din sectorul energetic, pentru a curăța solul și corpurile de apă și pentru a elimina deșeurile menajere. Apa grea obținută în timpul electrolizei este utilizată în domeniul energiei electrice în reactoarele nucleare.
Producția de hidrogen prin concentrație
Această metodă se bazează pe separarea unui element de amestecurile de gaze care îl conțin. Deci, cea mai mare parte a substanței produse în volume industriale este extrasă folosind reformarea cu abur a metanului. Hidrogenul extras în acest proces este utilizat în industria energetică, rafinarea petrolului, industria construcțiilor de rachete, precum și pentru producerea de îngrășăminte cu azot. Procesul de obținere a H2 se desfășoară în diferite moduri:
- ciclu scurt;
- criogenice;
- membrană.
Această din urmă metodă este considerată cea mai eficientă și mai puțin costisitoare.
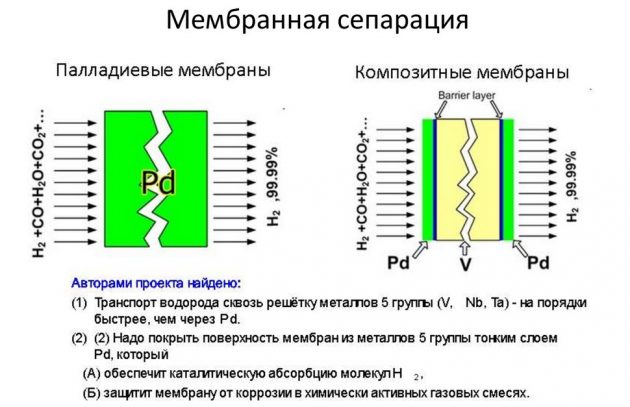

Condensare la temperatură scăzută
Această metodă de obținere a H2 constă în răcirea puternică a compușilor gazoși sub presiune. Ca urmare, acestea sunt transformate într-un sistem bifazat, care este separat ulterior printr-un separator într-o componentă lichidă și un gaz. Mediile lichide sunt utilizate pentru răcire:
- apă;
- etan sau propan lichefiat;
- amoniac lichid.


Această procedură nu este atât de ușoară pe cât pare. Nu va fi posibilă separarea curată a gazelor de hidrocarburi simultan. Unele componente vor pleca cu gaz preluat din compartimentul de separare, ceea ce nu este economic. Problema poate fi rezolvată prin răcirea profundă a materiei prime înainte de separare. Dar acest lucru necesită multă energie.
În sistemele moderne de condensare cu temperatură scăzută, sunt furnizate suplimentar coloane de demetanizare sau deetanizare. Faza gazoasă este îndepărtată din ultima etapă de separare, iar lichidul este trimis în coloana de distilare cu un flux de gaz brut după schimbul de căldură.
Metoda de adsorbție
În timpul adsorbției, pentru a elibera hidrogen, se folosesc adsorbanți - solide care absorb componentele necesare ale amestecului gazos. Carbonul activ, gelul de silicat, zeoliții sunt folosiți ca adsorbanți. Pentru a efectua acest proces, se folosesc dispozitive speciale - adsorbanți ciclici sau site moleculare. Atunci când este implementată sub presiune, această metodă poate recupera 85% hidrogen.
Dacă comparăm adsorbția cu condensul la temperatură scăzută, putem observa un cost material și operațional mai mic al procesului - în medie, cu 30 la sută. Hidrogenul este produs prin adsorbție pentru tehnica energiei electrice și cu ajutorul solvenților. Această metodă permite extragerea a 90% din H2 din amestecul gazos și obținerea produsului final cu o concentrație de hidrogen de până la 99,9%.